题目内容:
在一固定容积的密闭容器中进行如下反应:2SO (g)+O
(g)+O (g)
(g)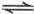 2SO
2SO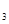 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO 、O
、O 、SO
、SO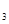 的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是A.10秒时,用O
的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是A.10秒时,用O 表示该反应的平均反应速率为0.01 mol/(L·s)B.当反应达平衡时,SO
表示该反应的平均反应速率为0.01 mol/(L·s)B.当反应达平衡时,SO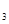 的物质的量可能为0.4 molC.当SO
的物质的量可能为0.4 molC.当SO 和O
和O 的生成速率之比为2:1时,达到该反应限度D.向容器内充人SO
的生成速率之比为2:1时,达到该反应限度D.向容器内充人SO ,可以提高反应速率
,可以提高反应速率
参考答案:
 (g)+O
(g)+O (g)
(g)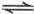 2SO
2SO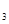 (g),已知反应进行到10秒时,SO
(g),已知反应进行到10秒时,SO 、O
、O 、SO
、SO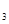 的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是A.10秒时,用O
的物质的量分别为0.2 mol、0.1 mol、0.2 mol,则下列说法正确的是A.10秒时,用O 表示该反应的平均反应速率为0.01 mol/(L·s)B.当反应达平衡时,SO
表示该反应的平均反应速率为0.01 mol/(L·s)B.当反应达平衡时,SO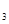 的物质的量可能为0.4 molC.当SO
的物质的量可能为0.4 molC.当SO 和O
和O 的生成速率之比为2:1时,达到该反应限度D.向容器内充人SO
的生成速率之比为2:1时,达到该反应限度D.向容器内充人SO ,可以提高反应速率
,可以提高反应速率